Publicado em 26 de agosto de 2022 às 10:02
A Anvisa aprovou nesta quinta-feira (25) a dispensa de registro para que o Ministério da Saúde importe e utilize no Brasil a vacina Jynneos / Imvanex, para imunização contra a monkeypox. Na decisão, por unanimidade, a Diretoria Colegiada aprovou a solicitação do Ministério da Saúde.
A autorização se aplica a vacina Jynneos (EUA) ou Imvanex (EMA) - (vacina contra varíola e Monkeypox, vírus vaccínia modificado, cepa Ankara) - , que apesar de ser o mesmo produto, possui nomes diferentes nos EUA e na Europa. A vacina da empresa Bavarian Nordic A/S é fabricada na Dinamarca e Alemanha.
O imunizante é destinado a adultos com idade igual ou superior a 18 anos e possui prazo de até 60 meses de validade quando conservada entre -60 a -40°C.
A dispensa temporária e excepcional se aplica somente ao Ministério da Saúde e terá validade de seis meses, desde que não seja expressamente revogada pela Anvisa.
Em seu voto, a diretora relatora Meiruze Freitas, destacou que a Monkeypox é causada por um vírus semelhante à varíola, portanto, espera-se que a vacina contra a varíola previna ou reduza a gravidade da infecção pela Monkeypox. Contudo, ressaltou a necessidade da condução de estudos de monitoramento para a confirmação da efetividade da vacina para a prevenção da Monkeypox.
Segundo o secretário de Vigilância em Saúde, Arnaldo Medeiros, a vacina a ser adquirida será de vírus não replicante. Em relação à compra de tratamentos, o Brasil negocia via OPAS/OMS e também com o fabricante, o antiviral Tecovirimat para reforçar o enfrentamento ao surto da doença. O antiviral é indicado para casos graves, com autorização para uso compassivo.
Em um primeiro momento, apenas profissionais de saúde que manipulam as amostras recolhidas de pacientes e pessoas que tiveram contato direto com doentes serão vacinados. Isso porque não existe por parte da Organização Mundial da Saúde recomendação para vacinação em massa para a varíola dos macacos. “Se houver indicação para imunização em massa em algum momento, para se ter vacina em escala, tem que existir outros parques fabris com capacidade para produzir essas doses”, destacou o ministro da saúde, Marcelo Queiroga, ao citar a limitação de produção em grande quantidade.
Para esta analise a Anvisa avaliou o Relatório de avaliação Agência Americana (FDA) para a vacina Jynneos, as informações públicas emitidas pela Agência Europeia de Medicamentos e Agência do Reino Unido, a bula, dizeres de rotulagem e demais documentos apresentados pelo Ministério da Saúde.
A documentação encaminhada pelo Ministério da Saúde é a mesma disponibilizada pelo FDA, sendo que o produto importado deverá corresponder as mesmas característica do pedido avaliado pela Anvisa.
A avaliação foi feita por equipe multidisciplinar composta por servidores concursados da Agência. Para a conclusão foi considerado as manifestações técnicas emitidas pelas seguintes áreas: Gerência-Geral de Produtos Biológicos, Radiofármacos, Sangue, Tecidos, Órgãos e Terapias Avançadas (GGBIO); Gerência de Avaliação de Eficácia e Segurança (GESEF/GGMED); Gerência-Geral de Inspeção e Fiscalização Sanitária (GGFIS): Gerência de Farmacovigilância (GFARM) e Gerência-Geral de Tecnologia e Serviços de Saúde (GGTES).
A autorização passa ser válida a partir da publicação do extrato da ata da DICOL no portal da Anvisa. Adicionalmente, será publicado no Diário Oficial da União - DOU, um Despacho com a decisão da Dicol.
No Brasil, até o momento, não há submissão de protocolo de ensaio clínico em vacinas para ser conduzido nacionalmente, tão pouco há protocolo submetido ou mesmo vacina já registrada pela Anvisa com a indicação de imunização contra Monkeypox.
Conforme previsto na RDC 747/2022 e para atender a emergência sanitária, a votação do processo ocorreu por meio o Circuito Deliberativo, utilizando o Sistema de Votação Eletrônica, com pauta prioritária para a deliberação.
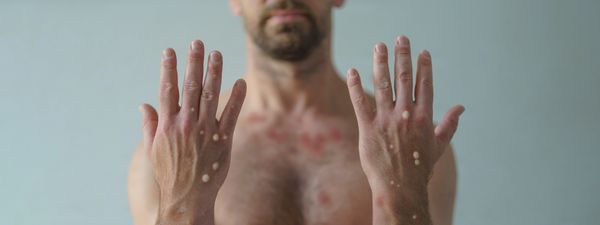
Anvisa aprovou a dispensa de registro para que o Ministério da Saúde importe e utilize no Brasil o medicamento Tecovirimat, para tratamento da doença monkeypox. A decisão da Diretoria Colegiada, por unanimidade, foi definida nesta quinta-feira (25/8), a partir da solicitação do Ministério da Saúde.
A autorização se aplica ao medicamento Tecovirimat, concentração de 200 mg, na forma farmacêutica cápsula dura, uso oral, prazo de validade de 84 meses e indicado para o tratamento de doenças causadas por Ortopoxvírus em adultos, adolescentes e crianças com peso mínimo de 13 kg.
O produto a ser importado é o mesmo autorizado nos EUA para a empresa SIGA Technologies, fabricado pela Catalent Pharma Solutions localizada em Winchester, Kentucky, Estados Unidos da América.
A dispensa temporária e excepcional se aplica somente ao Ministério da Saúde e terá validade de seis meses, desde que não seja expressamente revogada pela Anvisa.
A diretora relatora Meiruze Freitas, destacou em seu voto que o conhecimento prévio da Anvisa sobre o medicamento, resultado da comunicação e interação com as autoridades que avaliaram o medicamento, permitiu a rápida conclusão do processo. A diretora também pontuou que o acesso ao medicamento pode salvar vidas e controlar os danos da Monkeypox, especialmente para os pacientes em maiores riscos dos danos da doença.
Para esta análise foram avaliados o Relatório de avaliação da Agência Europeia (EMA) e da Agência Americana (FDA) para o medicamento Tecovirimat SIGA, a Bula e dizeres de rotulagem, o Parecer resumido de autorização de uso da Agência Europeia, Certificado de análise de controle de qualidade de lote, Relatório de inspeção do site de produção emitido pelo FDA, Instrução de uso do medicamento e dados da literatura científica.
A avaliação foi feita por equipe multidisciplinar composta por servidores concursados da Agência. Para a conclusão foi considerado as manifestações técnicas emitidas pelas seguintes áreas: Gerência Geral de Medicamentos (GGMED); Gerência de Avaliação de Qualidade de Medicamentos Sintéticos (GQMED/GGMED); Gerência de Avaliação de Eficácia e Segurança (GESEF/GGMED); Gerência-Geral de Inspeção e Fiscalização Sanitária (GGFIS): Gerência de Farmacovigilância (GFARM) e Gerência-Geral de Tecnologia e Serviços de Saúde (GGTES).
A autorização passa ser válida a partir da publicação do extrato da ata da DICOL no portal da Anvisa. Adicionalmente, será publicado no Diário Oficial da União - DOU, um Despacho com a decisão da Dicol.
Conforme previsto na RDC 747/2022 e para atender a emergência sanitária, a votação do processo ocorreu por meio o Circuito Deliberativo, utilizando o Sistema de Votação Eletrônica, com pauta prioritária para a deliberação.
No Brasil, até o momento, não há submissão de protocolo de ensaio clínico em medicamento para ser conduzido nacionalmente, tão pouco há protocolo submetido ou mesmo medicamento já registrado pela Anvisa com a indicação de tratamento da Monkeypox.
Notou alguma informação incorreta no conteúdo de A Gazeta? Nos ajude a corrigir o mais rápido possível! Clique no botão ao lado e envie sua mensagem.
Envie sua sugestão, comentário ou crítica diretamente aos editores de A Gazeta