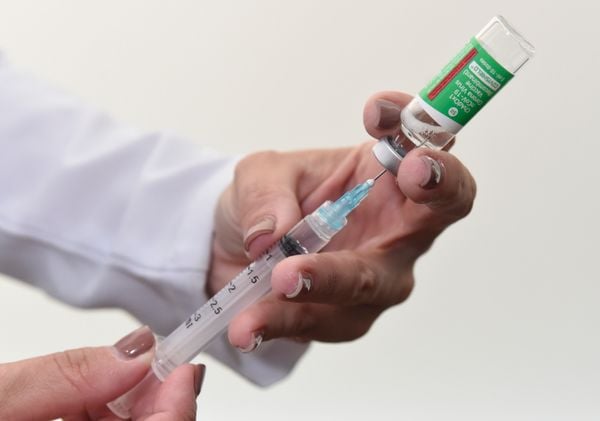
Ainda é cedo para uma análise definitiva, mas os dados monitorados até agora, obtidos no Brasil e em outros países, não apontam mudanças no perfil de segurança das vacinas contra o coronavírus. É o que afirma a gerente de monitoramento de produtos da Agência Nacional de Vigilância Sanitária (Anvisa), Suzie Gomes.
"Ainda é muito cedo (para conclusão), porque o número de pessoas vacinadas ainda é muito pequeno em relação a outras vacinas. Mas as suspeitas que são notificadas e registradas, mais as informações adicionais com outras autoridades regulatórias e com a base de dados da OMS (Organização Mundial de Saúde), não mostraram nenhuma alteração no perfil de segurança da vacina, o que é um ponto muito positivo", disse.
A declaração ocorreu em encontro com jornalistas nesta segunda-feira (22) para explicar como ocorre o processo de monitoramento de eventos adversos que podem estar ligados às vacinas contra a Covid.
Questionada sobre os dados brasileiros, Gomes disse que, embora o monitoramento tenha iniciado "já na primeira agulhada", o período de vacinação ainda é curto para que haja análise conclusiva. Ainda assim, os dados até o momento não sugerem alterações no perfil esperado, aponta.
"O que posso dizer é que não existe até o momento nenhum sinal [de problema] de segurança importante que desencadeie um processo regulatório ou ação regulatória", afirmou.
De acordo com a gerente, empresas devem entregar em breve o primeiro relatório de monitoramento de dados de riscos e benefícios de cada vacina. Em geral, esses dados são esperados a cada 90 dias --no caso de vacinas aprovadas para uso emergencial, a ideia é que um resumo seja enviado em prazo menor, a cada 30 dias. "Aí teremos mais um elemento para a análise", apontou.
Segundo Gomes, os eventos adversos mais frequentes têm sido dor de cabeça, febre e fadiga, já previstos em bula. Esse tipo de efeito é esperado, em geral, em 1 em cada 10 pessoas que toma as vacinas. "É algo absolutamente esperado, são reações previstas e que acontecem com outras vacinas e medicamentos", destacou.
Atualmente, o processo de monitoramento de eventos adversos ocorre por meio de sistemas do Ministério da Saúde, que recebe dados de unidades de saúde, e da Anvisa, por meio do Vigimed. Gomes disse que, por terem diferenças na definição e usarem classificações amplas, os dados não servem para fins estatísticos.
Segundo ela, é natural que os sistemas usem uma definição ampla de eventos adversos - ainda que, com isso, entrem para o monitoramento muitos casos que provavelmente não terão nenhuma ligação direta com a vacina.
"Evento adverso é qualquer ocorrência indesejada após a vacinação e que não necessariamente possui relação causal com o uso da vacina ou outro imunobiológico. Essa definição é absolutamente ampla. O sujeito chegou para receber a vacina, viu a agulha e desmaiou, é um evento adverso, ainda que não tenha relação com o produto", explicou.
No caso de eventos adversos considerados graves, o processo de investigação é iniciado em até 48 horas. A análise ocorre em grupos da agência e pode ser submetida a especialistas externos. Não há prazo final para conclusão, o que depende de cada caso - para casos menos complexos, a análise costuma ocorrer em até uma semana. Em outros, o acompanhamento pode durar até 12 meses.
A depender da conclusão, a agência pode adotar alertas ou tomar outras medidas, como recolher os produtos. Os dados observados até agora, porém, não apontam necessidade de nenhuma medida neste sentido. Também não tem sido observada nenhuma diferença significativa entre as vacinas neste processo, aponta.
Notou alguma informação incorreta no conteúdo de A Gazeta? Nos ajude a corrigir o mais rapido possível! Clique no botão ao lado e envie sua mensagem
Envie sua sugestão, comentário ou crítica diretamente aos editores de A Gazeta